向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸[高三][化学]
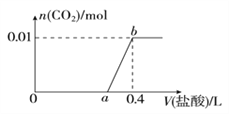
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )
A. 在0-a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
【答案】C
【解析】试题分析:A、在氢氧化钠与碳酸钠的混合液中,先发生氢离子与氢氧根离子的中和反应,再发生碳酸根离子与氢离子生成碳酸氢根离子的反应,所以在0-a范围内,不只发生中和反应,错误;B、a点2,溶液为氯化钠和碳酸氢钠溶液,所以ab段发生反应的离子方程式为:HCO3-+H+=H2O+CO2↑,错误;C、根据生成的二氧化碳的物质的量可知原溶液中有0.01mol的碳酸钠,0.01mol的碳酸钠与0.01mol的氢离子反应生成0.01mol的碳酸氢根离子,0.01mol的碳酸氢根离子需要0.01mol的氢离子反应生成0.01mol的二氧化碳,所以生成二氧化碳是消耗盐酸是0.01mol/0.1mol/L=0.1L,即0.4-a=0.1,所以a=0.3,正确;D、碳酸钠的物质的量是0.01mol,生成碳酸氢根离子消耗盐酸的体积是0.1L,则氢氧化钠消耗盐酸的体积是0.3-0.1=0.2L,所以氢氧化钠的物质的量是0.2L×0.1mol/L=0.02mol,原混合溶液中NaOH与Na2CO3的物质的量之比为2:1,错误,答案选C。
-
补全下面句子。(任选6空)(1)_,功在不舍。(荀子《劝学》)(2)...[高三][语文]
2021-12-22 -
阅读下文,完成下列小题。上枢密韩太尉书苏辙(1)辙生十有九年矣。其居家所与游者...[高三][语文]
2021-12-22 -
胡萝卜素是一种常用的食用色素,回答下列问题。(1)从胡萝卜中提取的胡萝素中...[高三][生物]
2021-12-22 -
阅读下文,完成下列小题。(1)刘章,汉高祖刘邦之孙,齐王刘肥次子,封朱虚侯...[高三][语文]
2021-12-22 -
家鸡属于鸟纲,是由原鸡长期驯化而来。回答下列问题。(1)...[高三][生物]
2021-12-22
